Cách tính số mol - Công thức và ứng dụng trong hóa học
Số mol là một khái niệm cơ bản trong hóa học, đo lường số lượng hạt (nguyên tử, phân tử, ion) trong một mẫu vật chất. Một mol chứa chính xác 6,022 x 10^23 hạt - con số này được gọi là số Avogadro. Đơn giản hóa, bạn có thể xem số mol như một "gói chuẩn" của các hạt vi mô.
Cách tính số mol là một kỹ năng quan trọng trong hóa học. Hãy cùng khám phá công thức cơ bản nhé:
Đơn giản phải không? Nhưng đừng vội! Chúng ta cần hiểu rõ từng thành phần trong công thức này.
Hãy cùng thực hành với một ví dụ cụ thể:
Ví dụ 1: Tính số mol của khí oxygen (O2)
Giả sử chúng ta có 64 gam khí oxygen (O2).
Bước 1: Xác định khối lượng mol của O2
Bước 2: Áp dụng công thức
Số mol = Khối lượng chất / Khối lượng mol
Số mol = 64 g / 32 g/mol = 2 mol
Vậy, 64 gam khí oxygen tương đương với 2 mol O2.
Ví dụ 2: Tính số mol của đồng sulfate (CuSO4)
Giả sử chúng ta có 40 gam đồng sulfate (CuSO4).
Bước 1: Xác định khối lượng mol của CuSO4
Bước 2: Áp dụng công thức
Số mol = 40 g / 159,5 g/mol ≈ 0,25 mol
Vậy, 40 gam đồng sulfate tương đương với khoảng 0,25 mol CuSO4.
Ví dụ 3: Tính số mol từ thể tích khí ở điều kiện chuẩn
Giả sử chúng ta có 44,8 lít khí carbon dioxide (CO2) ở điều kiện chuẩn.
Ở điều kiện chuẩn, 1 mol khí chiếm 22,4 lít. Do đó:
Số mol = Thể tích khí / 22,4 L/mol
Số mol = 44,8 L / 22,4 L/mol = 2 mol
Vậy, 44,8 lít CO2 ở điều kiện chuẩn tương đương với 2 mol CO2.
Ví dụ 4: Tính số mol từ số hạt
Giả sử chúng ta có 3,011 x 10^23 nguyên tử natri (Na).
Chúng ta biết rằng 1 mol chất chứa 6,022 x 10^23 hạt (số Avogadro). Do đó:
Số mol = Số hạt / Số Avogadro
Số mol = 3,011 x 10^23 / 6,022 x 10^23 = 0,5 mol
Vậy, 3,011 x 10^23 nguyên tử natri tương đương với 0,5 mol Na.
Ví dụ 5: Tính số mol của 36 gam nước (H2O)
Bước 1: Xác định khối lượng mol của H2O
Bước 2: Áp dụng công thức
Số mol = 36 g / 18 g/mol = 2 mol
Vậy, 36 gam nước tương đương với 2 mol H2O.
Bạn thấy đấy, với công thức và một chút tính toán, chúng ta đã dễ dàng xác định được số mol!
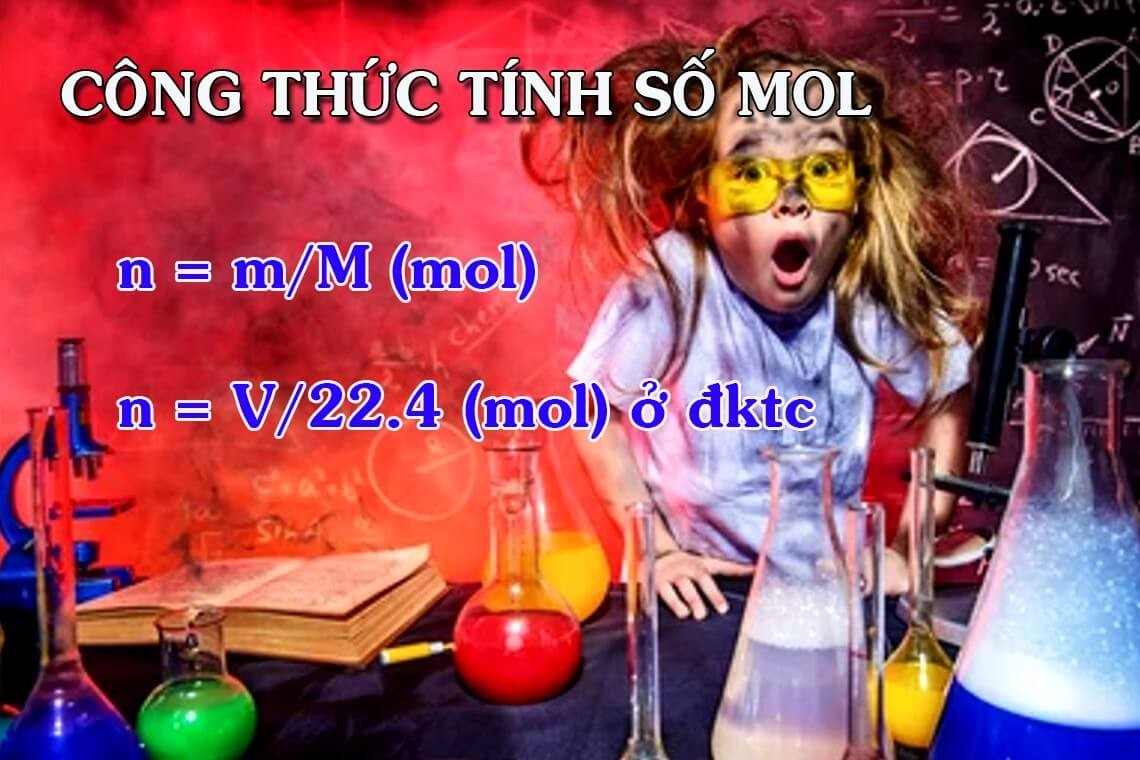
Khối lượng đóng vai trò quan trọng trong việc tính số mol. Có hai loại khối lượng chúng ta cần quan tâm:
Hiểu rõ sự khác biệt giữa hai khái niệm này sẽ giúp bạn tránh nhầm lẫn khi tính toán.
| Đặc điểm | Khối lượng | Khối lượng mol |
|---|---|---|
| Đơn vị | gam (g) | gam/mol (g/mol) |
| Ý nghĩa | Khối lượng thực tế của mẫu vật | Khối lượng của 1 mol chất |
| Cách xác định | Đo bằng cân | Tính từ nguyên tử khối |
Ví dụ:
Công thức hóa học không chỉ là một chuỗi chữ và số. Nó chứa đựng nhiều thông tin quan trọng:
Ví dụ: H2O
Hiểu rõ công thức hóa học giúp bạn tính toán khối lượng mol chính xác, từ đó tính được số mol một cách dễ dàng.
Tính số mol không chỉ là một bài tập trên giấy. Nó có nhiều ứng dụng thực tế trong hóa học:
Trong phản ứng hóa học, số mol giúp chúng ta xác định chính xác lượng chất cần dùng hoặc sản phẩm thu được.
Ví dụ: Phản ứng 2H2 + O2 → 2H2O
Bằng cách sử dụng số mol, chúng ta đảm bảo tỷ lệ chất tham gia phản ứng luôn chính xác.
Đối với chất khí, số mol có mối quan hệ đặc biệt với thể tích ở điều kiện chuẩn (0°C, 1 atm):
Thể tích = Số mol x 22,4 L/mol
Ví dụ: 3 mol CO2 sẽ chiếm thể tích là: 3 x 22,4 = 67,2 L (ở điều kiện chuẩn)
Điều này rất hữu ích trong các thí nghiệm và quy trình công nghiệp liên quan đến khí.
(Số mol) dùng để (tính toán) - (Nồng độ mol của dung dịch)
Nồng độ mol (còn gọi là nồng độ molar) là số mol chất tan trong 1 lít dung dịch. Công thức tính như sau:
Nồng độ mol (M) = Số mol chất tan / Thể tích dung dịch (L)
Ví dụ: Hòa tan 2 mol NaCl trong nước để được 500 mL dung dịch
Hiểu và áp dụng được những ứng dụng này, bạn sẽ thấy việc tính số mol không chỉ là lý thuyết suông, mà còn rất hữu ích trong thực tế!
Kết luận
Qua bài viết này, chúng ta đã cùng nhau khám phá cách tính số mol và ứng dụng của nó trong hóa học. Hãy cùng tổng kết lại những điểm chính:
Công thức tính số mol:
Số mol = Khối lượng chất / Khối lượng mol
Hiểu và thực hành tốt cách tính số mol sẽ giúp bạn có nền tảng vững chắc trong hóa học. Đừng ngại thử thách bản thân với nhiều bài tập đa dạng để củng cố kiến thức nhé!
Hãy nhớ rằng, mỗi công thức, mỗi phép tính đều mang trong mình một ý nghĩa sâu sắc về thế giới vật chất xung quanh chúng ta. Hóa học không chỉ là môn học trên lớp, mà còn là chìa khóa để hiểu rõ hơn về cuộc sống. Vì vậy, hãy giữ vững tinh thần tò mò và đam mê khám phá!
Chúc bạn thành công trong hành trình học hỏi và áp dụng kiến thức về số mol trong hóa học!
Hãy là người đầu tiên bình luận cho sản phẩm này
TIN TỨC LIÊN QUAN
0/5
Bạn có vấn đề cần tư vấn ?
Gửi câu hỏi